Vordering en ekonomiese analise van waterstofproduksie deur elektrolise van vaste oksiede
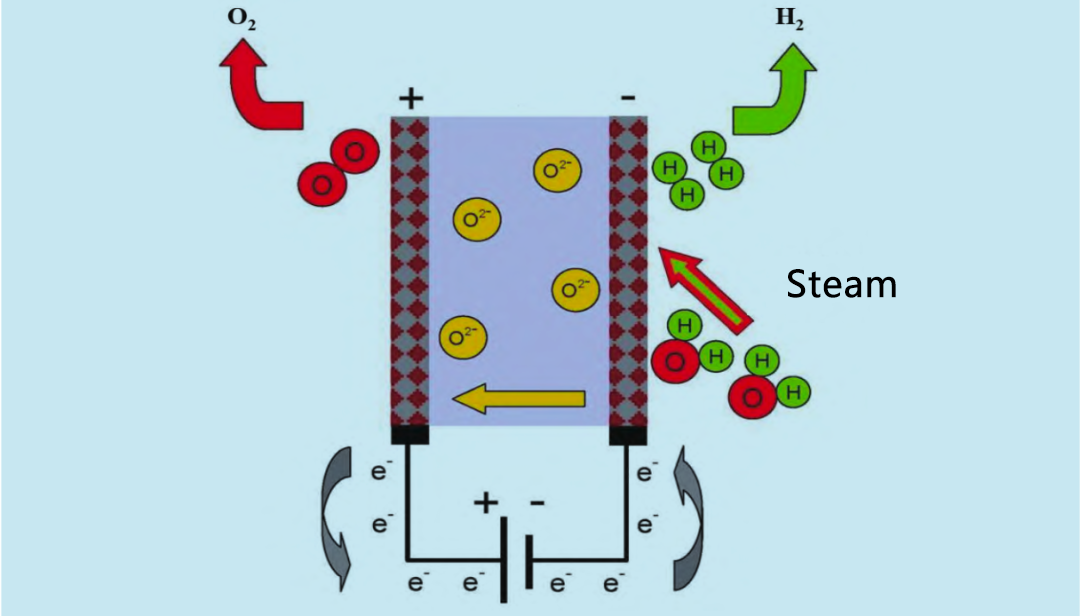
Vasteoksied-elektroliseerders (SOE) gebruik hoëtemperatuurwaterdamp (600 ~ 900°C) vir elektrolise, wat meer doeltreffend is as alkaliese elektroliseerders en PEM-elektroliseerders. In die 1960's het die Verenigde State en Duitsland begin om navorsing te doen oor hoëtemperatuurwaterdamp-SOE. Die werkbeginsel van die SOE-elektroliseerder word in Figuur 4 getoon. Herwinde waterstof en waterdamp betree die reaksiestelsel vanaf die anode. Die waterdamp word by die katode in waterstof geëlektroliseer. Die O2 wat deur die katode geproduseer word, beweeg deur die vaste elektroliet na die anode, waar dit herkombineer om suurstof te vorm en elektrone vry te stel.
Anders as alkaliese en protonuitruilmembraan-elektrolitiese selle, reageer die SOE-elektrode met waterdampkontak en staar die uitdaging in die gesig om die koppelvlakarea tussen die elektrode en waterdampkontak te maksimeer. Daarom het die SOE-elektrode oor die algemeen 'n poreuse struktuur. Die doel van waterdampelektrolise is om die energie-intensiteit te verminder en die bedryfskoste van konvensionele vloeibare waterelektrolise te verlaag. Trouens, hoewel die totale energievereiste van die waterontbindingsreaksie effens toeneem met toenemende temperatuur, neem die elektriese energievereiste aansienlik af. Soos die elektrolitiese temperatuur toeneem, word 'n deel van die benodigde energie as hitte verskaf. Die SOE is in staat om waterstof te produseer in die teenwoordigheid van 'n hoëtemperatuur-hittebron. Aangesien hoëtemperatuur-gasverkoelde kernreaktore tot 950°C verhit kan word, kan kernenergie as 'n energiebron vir die SOE gebruik word. Terselfdertyd toon die navorsing dat hernubare energie soos geotermiese energie ook die potensiaal het as die hittebron van stoomelektrolise. Deur teen hoë temperatuur te werk, kan die batteryspanning verminder word en die reaksiespoed verhoog word, maar dit staar ook die uitdaging van materiaaltermiese stabiliteit en verseëling in die gesig. Daarbenewens is die gas wat deur die katode geproduseer word 'n waterstofmengsel, wat verder geskei en gesuiwer moet word, wat die koste verhoog in vergelyking met konvensionele vloeibare waterelektrolise. Die gebruik van protongeleidende keramiek, soos stronsiumsirkonaat, verminder die koste van SOE. Stronsiumsirkonaat toon uitstekende protongeleidingsvermoë by ongeveer 700°C, en is bevorderlik vir die katode om hoë suiwerheid waterstof te produseer, wat die stoomelektrolise-toestel vereenvoudig.
Yan et al. [6] het berig dat 'n sirkonium-keramiekbuis, gestabiliseer deur kalsiumoksied, as SOE van die ondersteunende struktuur gebruik is, met die buitenste oppervlak bedek met dun (minder as 0.25 mm) poreuse lantaanperovskiet as anode, en Ni/Y2O3 stabiele kalsiumoksied-kermet as katode. By 1000°C, 0.4A/cm2 en 39.3W insetkrag, is die waterstofproduksiekapasiteit van die eenheid 17.6NL/h. Die nadeel van SOE is die oorspanning as gevolg van hoë ohm-verliese wat algemeen voorkom by die verbindings tussen selle, en die hoë oorspanningskonsentrasie as gevolg van die beperkings van dampdiffusie-transport. In onlangse jare het planêre elektrolitiese selle baie aandag getrek [7-8]. In teenstelling met buisvormige selle, maak plat selle vervaardiging meer kompak en verbeter waterstofproduksiedoeltreffendheid [6]. Tans is die grootste struikelblok vir die industriële toepassing van SOE die langtermynstabiliteit van die elektrolitiese sel [8], en die probleme van elektrodeveroudering en deaktivering kan veroorsaak word.
Plasingstyd: 6 Februarie 2023