Voortgang en economische analyse van waterstofproductie door elektrolyse van vaste oxiden
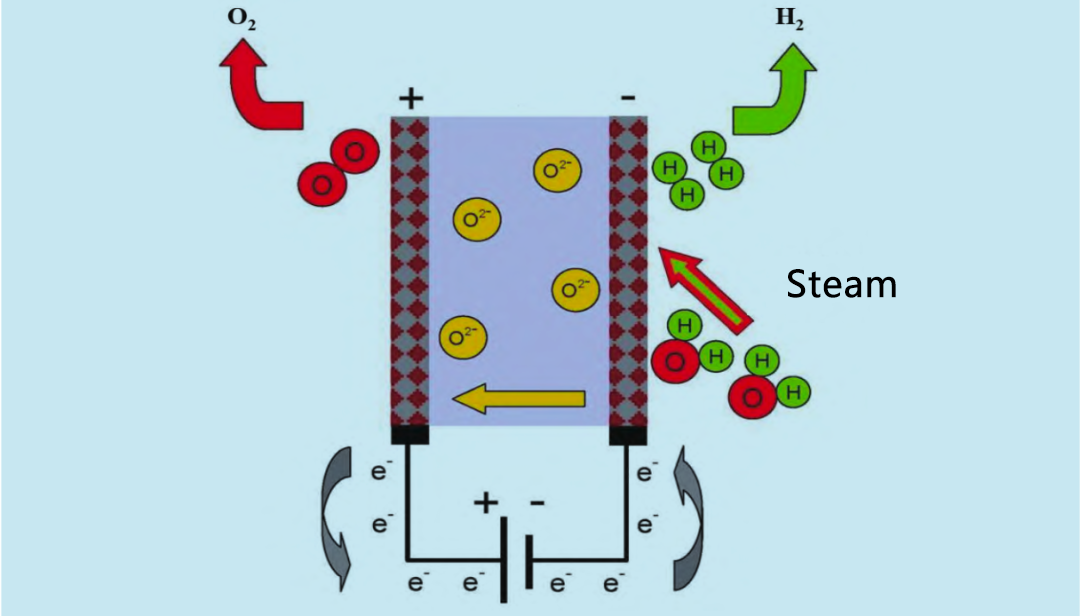
Vaste-oxide-elektrolysers (SOE) gebruiken waterdamp met hoge temperatuur (600 ~ 900 °C) voor elektrolyse, wat efficiënter is dan alkalische elektrolysers en PEM-elektrolysers. In de jaren 60 begonnen de Verenigde Staten en Duitsland onderzoek te doen naar SOE's met waterdamp met hoge temperatuur. Het werkingsprincipe van de SOE-elektrolyser is weergegeven in figuur 4. Gerecycleerde waterstof en waterdamp komen via de anode in het reactiesysteem terecht. De waterdamp wordt aan de kathode geëlektrolyseerd tot waterstof. De door de kathode geproduceerde O₂ beweegt door de vaste elektrolyt naar de anode, waar het recombineert tot zuurstof en elektronen vrijgeeft.
In tegenstelling tot alkalische en protonenuitwisselingsmembraanelektrolytische cellen reageert de SOE-elektrode met waterdampcontact en staat hij voor de uitdaging om het grensvlak tussen de elektrode en het waterdampcontact te maximaliseren. Daarom heeft de SOE-elektrode over het algemeen een poreuze structuur. Het doel van waterdampelektrolyse is om de energie-intensiteit te verminderen en de bedrijfskosten van conventionele vloeibaar-waterelektrolyse te verlagen. Hoewel de totale energiebehoefte van de waterontledingsreactie licht toeneemt met toenemende temperatuur, neemt de elektrische energiebehoefte aanzienlijk af. Naarmate de elektrolytische temperatuur stijgt, wordt een deel van de benodigde energie geleverd als warmte. De SOE kan waterstof produceren in aanwezigheid van een hogetemperatuurwarmtebron. Omdat gasgekoelde kernreactoren met hoge temperatuur kunnen worden verwarmd tot 950 °C, kan kernenergie worden gebruikt als energiebron voor de SOE. Tegelijkertijd toont het onderzoek aan dat hernieuwbare energie, zoals geothermische energie, ook de potentie heeft om als warmtebron voor stoomelektrolyse te dienen. Werken bij hoge temperaturen kan de batterijspanning verlagen en de reactiesnelheid verhogen, maar het brengt ook de uitdaging met zich mee van thermische stabiliteit en afdichting van het materiaal. Bovendien is het door de kathode geproduceerde gas een waterstofmengsel, dat verder moet worden gescheiden en gezuiverd, wat de kosten verhoogt ten opzichte van conventionele elektrolyse met vloeibaar water. Het gebruik van protongeleidende keramische materialen, zoals strontiumzirconaat, verlaagt de kosten van SOE. Strontiumzirconaat vertoont een uitstekende protongeleidbaarheid bij ongeveer 700 °C en is geschikt voor de kathode om waterstof met een hoge zuiverheid te produceren, wat de stoomelektrolyse vereenvoudigt.
Yan et al. [6] meldden dat een keramische buis van zirkonia, gestabiliseerd door calciumoxide, werd gebruikt als SOE van de ondersteunende structuur, het buitenoppervlak werd bedekt met dun (minder dan 0,25 mm) poreus lanthaanperovskiet als anode en Ni/Y2O3 stabiel calciumoxide cermet als kathode. Bij 1000°C, 0,4A/cm2 en 39,3W ingangsvermogen is de waterstofproductiecapaciteit van de eenheid 17,6NL/h. Het nadeel van SOE is de overspanning als gevolg van hoge ohmse verliezen die veel voorkomen bij de onderlinge verbindingen tussen cellen, en de hoge overspanningsconcentratie als gevolg van de beperkingen van dampdiffusietransport. De laatste jaren hebben vlakke elektrolytische cellen veel aandacht getrokken [7-8]. In tegenstelling tot buisvormige cellen maken platte cellen de productie compacter en verbeteren ze de waterstofproductie-efficiëntie [6]. Op dit moment is het grootste obstakel voor de industriële toepassing van SOE de stabiliteit op de lange termijn van de elektrolytische cel [8], en kunnen er problemen ontstaan door veroudering en deactivering van de elektroden.
Plaatsingstijd: 06-02-2023