همانطور که در شکل 3 نشان داده شده است، سه تکنیک غالب با هدف ارائه تک کریستال SiC با کیفیت و راندمان بالا وجود دارد: اپیتاکسی فاز مایع (LPE)، انتقال بخار فیزیکی (PVT) و رسوب بخار شیمیایی در دمای بالا (HTCVD). PVT یک فرآیند جاافتاده برای تولید تک کریستال SiC است که به طور گسترده در تولیدکنندگان اصلی ویفر مورد استفاده قرار میگیرد.
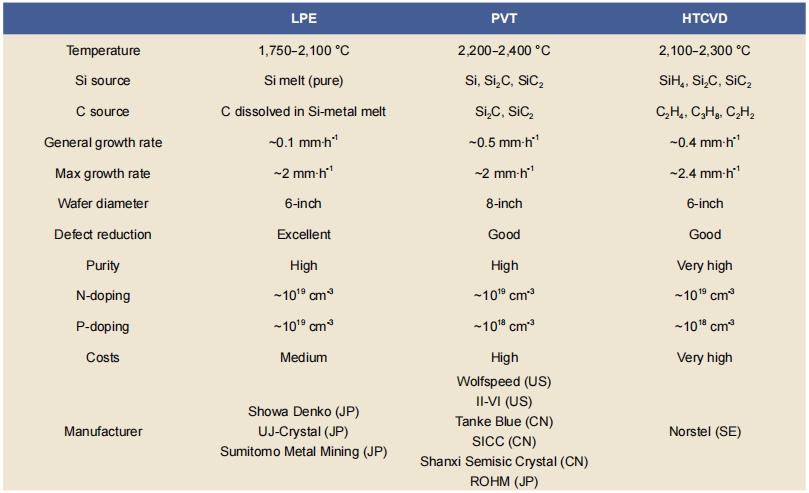
با این حال، هر سه فرآیند به سرعت در حال تکامل و نوآوری هستند. هنوز نمیتوان پیشبینی کرد که کدام فرآیند در آینده به طور گسترده مورد استفاده قرار خواهد گرفت. به طور خاص، در سالهای اخیر گزارش شده است که تک کریستال SiC با کیفیت بالا از طریق رشد محلول با سرعت قابل توجهی تولید میشود. رشد تودهای SiC در فاز مایع به دمای پایینتری نسبت به فرآیند تصعید یا رسوب نیاز دارد و برتری خود را در تولید زیرلایههای SiC نوع P نشان میدهد (جدول 3) [33، 34].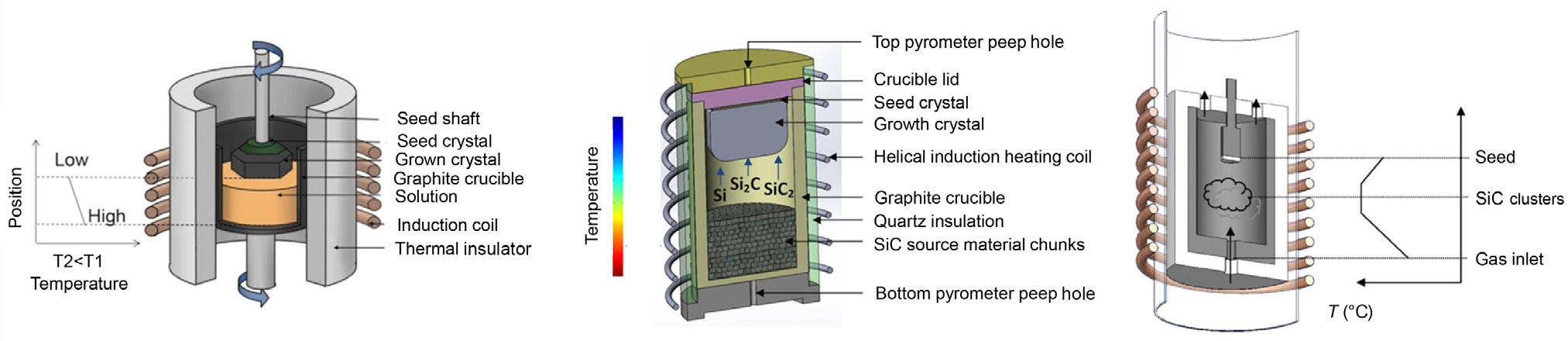
شکل 3: شماتیک سه تکنیک غالب رشد تک بلور SiC: (الف) اپیتاکسی فاز مایع؛ (ب) انتقال فیزیکی بخار؛ (ج) رسوب بخار شیمیایی در دمای بالا
جدول 3: مقایسه LPE، PVT و HTCVD برای رشد تک بلورهای SiC [33، 34]
رشد محلول یک فناوری استاندارد برای تهیه نیمهرساناهای مرکب است [36]. از دهه 1960، محققان تلاش کردهاند تا یک کریستال را در محلول توسعه دهند [37]. پس از توسعه این فناوری، میتوان فوق اشباع سطح رشد را به خوبی کنترل کرد، که این امر روش محلول را به یک فناوری امیدوارکننده برای به دست آوردن شمشهای تک کریستالی با کیفیت بالا تبدیل میکند.
برای رشد محلولی تک کریستال SiC، منبع Si از مذاب Si بسیار خالص ناشی میشود در حالی که بوته گرافیتی دو هدف را دنبال میکند: گرمکن و منبع حلشونده C. تک کریستالهای SiC تحت نسبت استوکیومتری ایدهآل، زمانی که نسبت C و Si نزدیک به 1 باشد، احتمال رشد بیشتری دارند که نشان دهنده چگالی نقص کمتر است [28]. با این حال، در فشار اتمسفر، SiC هیچ نقطه ذوبی نشان نمیدهد و مستقیماً از طریق تبخیر در دماهای بالاتر از حدود 2000 درجه سانتیگراد تجزیه میشود. طبق انتظارات نظری، ذوب SiC فقط میتواند تحت شرایط شدید تشکیل شود، همانطور که از نمودار فاز دوتایی Si-C (شکل 4) دیده میشود که در گرادیان دما و سیستم محلول قرار دارد. هرچه C در مذاب Si بالاتر باشد، از 1 اتمسفر تا 13 اتمسفر متغیر است. فوق اشباع C محرک، سرعت رشد را سریعتر میکند، در حالی که نیروی کم C رشد، فوق اشباع C است که تحت فشار 109 پاسکال و دمای بالاتر از 3200 درجه سانتیگراد قرار دارد. فوق اشباع بودن میتواند سطح صافی ایجاد کند [22، 36-38]. در دمای بین 1400 تا 2800 درجه سانتیگراد، حلالیت کربن در مذاب سیلیکون از 1 درصد اتمی تا 13 درصد اتمی متغیر است. نیروی محرکه رشد، فوق اشباع بودن کربن است که تحت تأثیر گرادیان دما و سیستم محلول قرار دارد. هرچه فوق اشباع بودن کربن بیشتر باشد، سرعت رشد بیشتر است، در حالی که فوق اشباع بودن کم کربن سطح صافی ایجاد میکند [22، 36-38].
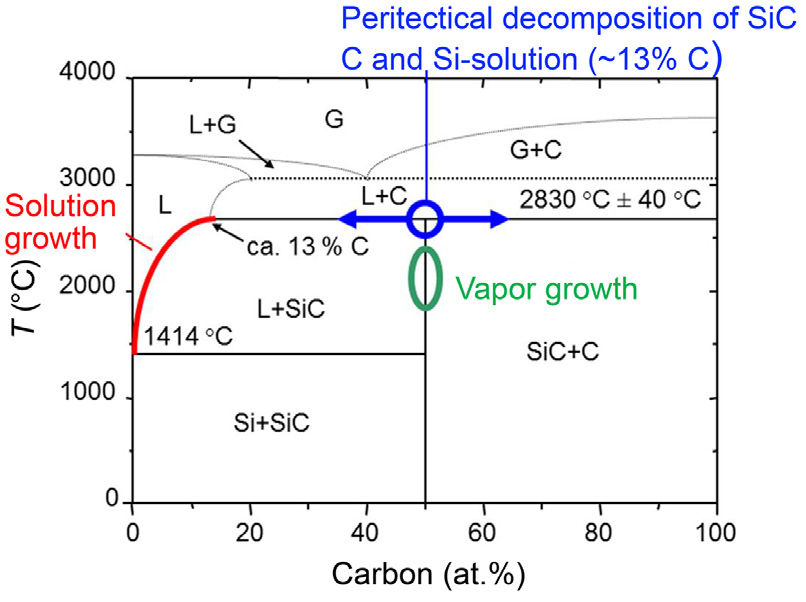
شکل 4: نمودار فاز دوتایی Si-C [40]
آلایش عناصر فلزات واسطه یا عناصر خاکی کمیاب نه تنها به طور مؤثر دمای رشد را کاهش میدهد، بلکه به نظر میرسد تنها راه برای بهبود چشمگیر حلالیت کربن در مذاب Si باشد. افزودن فلزات گروه واسطه، مانند Ti [8، 14-16، 19، 40-52]، Cr [29، 30، 43، 50، 53-75]، Co [63، 76]، Fe [77-80] و غیره یا فلزات خاکی کمیاب، مانند Ce [81]، Y [82]، Sc و غیره به مذاب Si اجازه میدهد تا حلالیت کربن در حالت نزدیک به تعادل ترمودینامیکی از 50 درصد اتمی فراتر رود. علاوه بر این، تکنیک LPE برای آلایش نوع P SiC مطلوب است که میتواند با آلیاژ کردن Al به مذاب SiC حاصل شود.
حلال [50، 53، 56، 59، 64، 71-73، 82، 83]. با این حال، افزودن آلومینیوم منجر به افزایش مقاومت ویژه تک بلورهای SiC نوع P میشود [49، 56]. جدا از رشد نوع N تحت آلایش نیتروژن،
رشد محلول عموماً در اتمسفر گاز بیاثر انجام میشود. اگرچه هلیوم (He) گرانتر از آرگون است، اما به دلیل ویسکوزیته پایینتر و رسانایی حرارتی بالاتر (8 برابر آرگون) مورد توجه بسیاری از محققان قرار گرفته است [85]. نرخ مهاجرت و محتوای Cr در 4H-SiC در اتمسفر He و Ar مشابه است، ثابت شده است که رشد تحت Heres به دلیل اتلاف گرمای بیشتر نگهدارنده بذر، منجر به نرخ رشد بالاتری نسبت به رشد تحت Ar میشود [68]. He مانع از تشکیل حفرهها در داخل کریستال رشد یافته و هستهزایی خود به خودی در محلول میشود، بنابراین میتوان مورفولوژی سطح صافی را به دست آورد [86].
این مقاله به معرفی توسعه، کاربردها و خواص قطعات SiC و سه روش اصلی برای رشد تک بلور SiC میپردازد. در بخشهای بعدی، تکنیکهای رشد محلول فعلی و پارامترهای کلیدی مربوطه بررسی شدند. در نهایت، چشماندازی ارائه شد که چالشها و کارهای آینده در مورد رشد حجمی تک بلورهای SiC از طریق روش محلول را مورد بحث قرار میدهد.
زمان ارسال: ژوئیه-01-2024