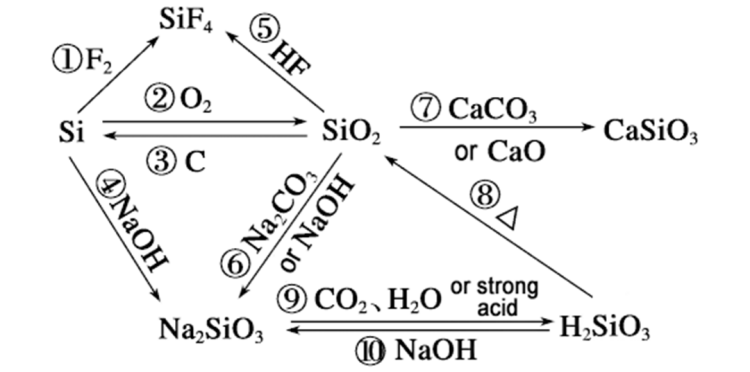
Poukisa vitès reyaksyon ansilikonepi idroksid sodyòm ka depase idroksid Silisyòm nan, yo ka analize li nan aspè sa yo:
Diferans nan enèji lyezon chimik
▪ Reyaksyon Silisyòm ak idroksid sodyòm: Lè Silisyòm reyaji avèk idroksid sodyòm, enèji lyezon Si-Si ant atòm Silisyòm yo se sèlman 176kJ/mol. Lyezon Si-Si a kase pandan reyaksyon an, sa ki relativman pi fasil pou kase. Nan yon pwen de vi sinetik, reyaksyon an pi fasil pou kontinye.
▪ Reyaksyon diyoksid Silisyòm ak idroksid sodyòm: Enèji lyezon Si-O ant atòm Silisyòm ak atòm oksijèn nan diyoksid Silisyòm se 460kJ/mol, ki relativman wo. Li pran plis enèji pou kraze lyezon Si-O a pandan reyaksyon an, kidonk reyaksyon an relativman difisil pou fèt epi vitès reyaksyon an ralanti.
Mekanis reyaksyon diferan
▪ Silisyòm reyaji avèk idroksid sodyòm: Silisyòm reyaji avèk idroksid sodyòm dabò lè li reyaji avèk dlo pou jenere idwojèn ak asid silisik, answit asid silisik reyaji avèk idroksid sodyòm pou jenere silikat sodyòm ak dlo. Pandan reyaksyon sa a, reyaksyon ant Silisyòm ak dlo a libere chalè, sa ki ka ankouraje mouvman molekilè, kidonk kreye yon pi bon anviwònman sinetik pou reyaksyon an epi akselere vitès reyaksyon an.
▪ Diyoksid Silisyòm reyaji avèk idroksid sodyòm: Diyoksid Silisyòm reyaji avèk idroksid sodyòm dabò lè li reyaji avèk dlo pou jenere asid silisik, answit asid silisik reyaji avèk idroksid sodyòm pou jenere silikat sodyòm. Reyaksyon ant diyoksid Silisyòm ak dlo a trè dousman, epi pwosesis reyaksyon an fondamantalman pa degaje chalè. Nan yon pwen de vi sinetik, li pa fezab pou yon reyaksyon rapid.
Diferan estrikti materyèl
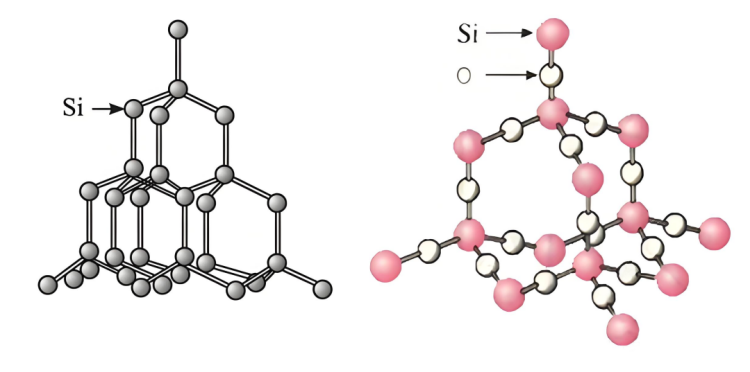
▪ Estrikti Silisyòm:Silisyòmgen yon sèten estrikti kristal, epi gen sèten espas ak entèraksyon relativman fèb ant atòm yo, sa ki fè li pi fasil pou solisyon idroksid sodyòm kontakte epi reyaji ak atòm Silisyòm yo.
▪ Estriktisilikondiyoksid:silikondiyoksid gen yon estrikti rezo espasyal ki estab.SilisyòmAtòm yo ak atòm oksijèn yo lye byen sere pa lyezon kovalan pou fòme yon estrikti kristal ki di e ki estab. Li difisil pou solisyon idwoksid sodyòm penetre anndan li epi kontakte nèt atòm silikon yo, sa ki lakòz difikilte pou reyaksyon rapid. Se sèlman atòm silikon ki sou sifas patikil diyoksid silikon yo ki ka reyaji avèk idwoksid sodyòm, sa ki limite vitès reyaksyon an.
Efè kondisyon yo
▪ Reyaksyon Silisyòm ak idroksid sodyòm: Anba kondisyon chofaj, vitès reyaksyon Silisyòm ak solisyon idroksid sodyòm lan pral akselere anpil, epi reyaksyon an ka jeneralman dewoule san pwoblèm nan tanperati ki wo.
▪ Reyaksyon diyoksid Silisyòm ak idroksid sodyòm: Reyaksyon diyoksid Silisyòm ak solisyon idroksid sodyòm trè dousman nan tanperati chanm. Anjeneral, vitès reyaksyon an ap amelyore nan kondisyon difisil tankou tanperati ki wo ak solisyon idroksid sodyòm konsantre.
Dat piblikasyon: 10 Desanm 2024