Γιατί ο ρυθμός αντίδρασης τουπυρίτιοκαι το υδροξείδιο του νατρίου μπορεί να ξεπεράσει αυτό του διοξειδίου του πυριτίου μπορεί να αναλυθεί από τις ακόλουθες απόψεις:
Διαφορά στην ενέργεια χημικού δεσμού
▪ Αντίδραση πυριτίου και υδροξειδίου του νατρίου: Όταν το πυρίτιο αντιδρά με υδροξείδιο του νατρίου, η ενέργεια του δεσμού Si-Si μεταξύ των ατόμων πυριτίου είναι μόνο 176kJ/mol. Ο δεσμός Si-Si σπάει κατά τη διάρκεια της αντίδρασης, κάτι που είναι σχετικά πιο εύκολο να διασπαστεί. Από κινητική άποψη, η αντίδραση προχωρά πιο εύκολα.
▪ Αντίδραση διοξειδίου του πυριτίου και υδροξειδίου του νατρίου: Η ενέργεια του δεσμού Si-O μεταξύ ατόμων πυριτίου και ατόμων οξυγόνου στο διοξείδιο του πυριτίου είναι 460kJ/mol, η οποία είναι σχετικά υψηλή. Απαιτείται μεγαλύτερη ενέργεια για να διασπαστεί ο δεσμός Si-O κατά τη διάρκεια της αντίδρασης, επομένως η αντίδραση είναι σχετικά δύσκολο να συμβεί και ο ρυθμός της αντίδρασης είναι αργός.
Διαφορετικοί μηχανισμοί αντίδρασης
▪ Το πυρίτιο αντιδρά με υδροξείδιο του νατρίου: Το πυρίτιο αντιδρά πρώτα με υδροξείδιο του νατρίου αντιδρώντας με νερό για να παράγει υδρογόνο και πυριτικό οξύ, και στη συνέχεια το πυριτικό οξύ αντιδρά με υδροξείδιο του νατρίου για να παράγει πυριτικό νάτριο και νερό. Κατά τη διάρκεια αυτής της αντίδρασης, η αντίδραση μεταξύ πυριτίου και νερού απελευθερώνει θερμότητα, η οποία μπορεί να προωθήσει την μοριακή κίνηση, δημιουργώντας έτσι ένα καλύτερο κινητικό περιβάλλον για την αντίδραση και επιταχύνοντας τον ρυθμό της αντίδρασης.
▪ Το διοξείδιο του πυριτίου αντιδρά με υδροξείδιο του νατρίου: Το διοξείδιο του πυριτίου αντιδρά πρώτα με υδροξείδιο του νατρίου αντιδρώντας με νερό για να παράγει πυριτικό οξύ, και στη συνέχεια το πυριτικό οξύ αντιδρά με υδροξείδιο του νατρίου για να παράγει πυριτικό νάτριο. Η αντίδραση μεταξύ διοξειδίου του πυριτίου και νερού είναι εξαιρετικά αργή και η διαδικασία της αντίδρασης ουσιαστικά δεν απελευθερώνει θερμότητα. Από κινητική άποψη, δεν ευνοεί μια ταχεία αντίδραση.
Διαφορετικές δομές υλικών
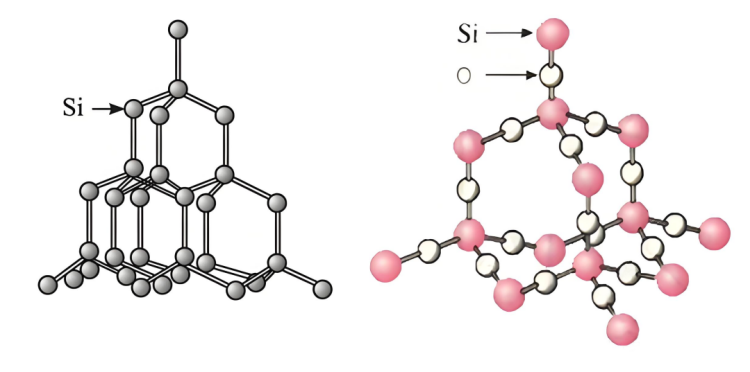
▪ Δομή πυριτίου:Πυρίτιοέχει μια συγκεκριμένη κρυσταλλική δομή και υπάρχουν ορισμένα κενά και σχετικά ασθενείς αλληλεπιδράσεις μεταξύ των ατόμων, γεγονός που διευκολύνει την επαφή και την αντίδραση του διαλύματος υδροξειδίου του νατρίου με άτομα πυριτίου.
▪ Δομή τουπυρίτιοδιοξίδιο:πυρίτιοΤο διοξείδιο έχει μια σταθερή χωρική δομή δικτύου.ΠυρίτιοΤα άτομα και τα άτομα οξυγόνου συνδέονται στενά με ομοιοπολικούς δεσμούς για να σχηματίσουν μια σκληρή και σταθερή κρυσταλλική δομή. Είναι δύσκολο για το διάλυμα υδροξειδίου του νατρίου να διεισδύσει στο εσωτερικό του και να έρθει σε πλήρη επαφή με άτομα πυριτίου, με αποτέλεσμα να δυσκολεύεται η ταχεία αντίδραση. Μόνο άτομα πυριτίου στην επιφάνεια των σωματιδίων διοξειδίου του πυριτίου μπορούν να αντιδράσουν με υδροξείδιο του νατρίου, περιορίζοντας τον ρυθμό αντίδρασης.
Επίδραση των συνθηκών
▪ Αντίδραση πυριτίου με υδροξείδιο του νατρίου: Υπό συνθήκες θέρμανσης, ο ρυθμός αντίδρασης πυριτίου με διάλυμα υδροξειδίου του νατρίου θα επιταχυνθεί σημαντικά και η αντίδραση μπορεί γενικά να προχωρήσει ομαλά σε υψηλές θερμοκρασίες.
▪ Αντίδραση διοξειδίου του πυριτίου με υδροξείδιο του νατρίου: Η αντίδραση διοξειδίου του πυριτίου με διάλυμα υδροξειδίου του νατρίου είναι πολύ αργή σε θερμοκρασία δωματίου. Συνήθως, ο ρυθμός αντίδρασης βελτιώνεται υπό σκληρές συνθήκες, όπως υψηλή θερμοκρασία και πυκνό διάλυμα υδροξειδίου του νατρίου.
Ώρα δημοσίευσης: 10 Δεκεμβρίου 2024