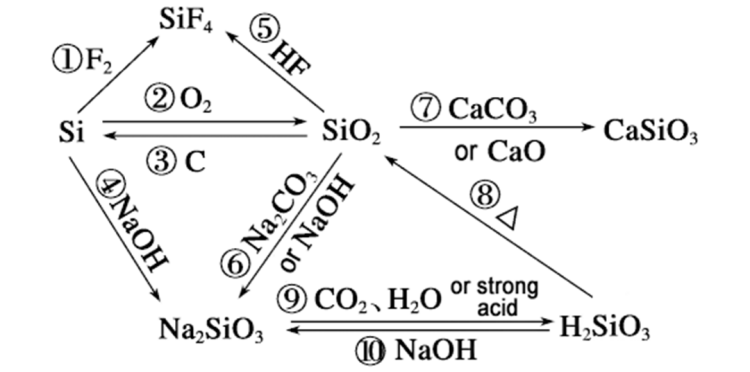
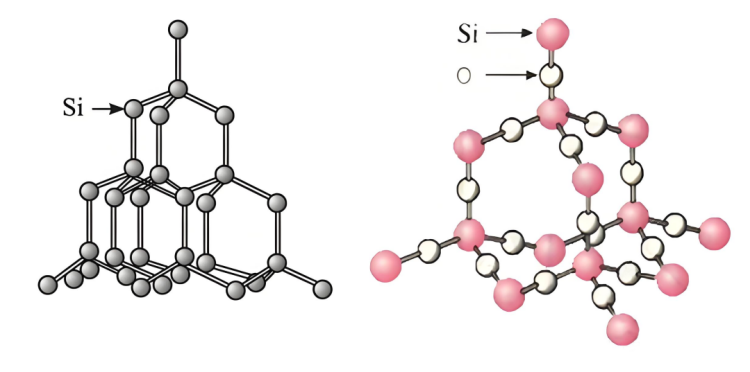
પ્રતિક્રિયા દર શા માટેસિલિકોનઅને સોડિયમ હાઇડ્રોક્સાઇડ સિલિકોન ડાયોક્સાઇડ કરતા વધી શકે છે તેનું વિશ્લેષણ નીચેના પાસાઓથી કરી શકાય છે:
રાસાયણિક બંધન ઊર્જામાં તફાવત
▪ સિલિકોન અને સોડિયમ હાઇડ્રોક્સાઇડની પ્રતિક્રિયા: જ્યારે સિલિકોન સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા આપે છે, ત્યારે સિલિકોન પરમાણુઓ વચ્ચે Si-Si બોન્ડ ઊર્જા માત્ર 176kJ/mol હોય છે. પ્રતિક્રિયા દરમિયાન Si-Si બોન્ડ તૂટી જાય છે, જેને તોડવું પ્રમાણમાં સરળ છે. ગતિશીલ દ્રષ્ટિકોણથી, પ્રતિક્રિયા આગળ વધવી સરળ છે.
▪ સિલિકોન ડાયોક્સાઇડ અને સોડિયમ હાઇડ્રોક્સાઇડની પ્રતિક્રિયા: સિલિકોન ડાયોક્સાઇડમાં સિલિકોન પરમાણુઓ અને ઓક્સિજન પરમાણુઓ વચ્ચે Si-O બોન્ડ ઊર્જા 460kJ/mol છે, જે પ્રમાણમાં ઊંચી છે. પ્રતિક્રિયા દરમિયાન Si-O બોન્ડ તોડવા માટે વધુ ઊર્જાની જરૂર પડે છે, તેથી પ્રતિક્રિયા થવી પ્રમાણમાં મુશ્કેલ છે અને પ્રતિક્રિયા દર ધીમો છે.
વિવિધ પ્રતિક્રિયા પદ્ધતિઓ
▪ સિલિકોન સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા આપે છે: સિલિકોન સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા આપે છે અને પહેલા પાણી સાથે પ્રતિક્રિયા કરીને હાઇડ્રોજન અને સિલિકિક એસિડ ઉત્પન્ન કરે છે, પછી સિલિકિક એસિડ સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા કરીને સોડિયમ સિલિકેટ અને પાણી ઉત્પન્ન કરે છે. આ પ્રતિક્રિયા દરમિયાન, સિલિકોન અને પાણી વચ્ચેની પ્રતિક્રિયા ગરમી મુક્ત કરે છે, જે પરમાણુ ગતિને પ્રોત્સાહન આપી શકે છે, જેનાથી પ્રતિક્રિયા માટે વધુ સારું ગતિ વાતાવરણ બને છે અને પ્રતિક્રિયા દર ઝડપી બને છે.
▪ સિલિકોન ડાયોક્સાઇડ સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા આપે છે: સિલિકોન ડાયોક્સાઇડ સૌપ્રથમ પાણી સાથે પ્રતિક્રિયા કરીને સિલિકિક એસિડ ઉત્પન્ન કરે છે, પછી સિલિકિક એસિડ સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા કરીને સોડિયમ સિલિકેટ ઉત્પન્ન કરે છે. સિલિકોન ડાયોક્સાઇડ અને પાણી વચ્ચેની પ્રતિક્રિયા અત્યંત ધીમી હોય છે, અને પ્રતિક્રિયા પ્રક્રિયા મૂળભૂત રીતે ગરમી છોડતી નથી. ગતિશીલ દ્રષ્ટિકોણથી, તે ઝડપી પ્રતિક્રિયા માટે અનુકૂળ નથી.
વિવિધ સામગ્રી રચનાઓ
▪ સિલિકોન રચના:સિલિકોનતેમાં ચોક્કસ સ્ફટિક માળખું હોય છે, અને અણુઓ વચ્ચે ચોક્કસ ગાબડા અને પ્રમાણમાં નબળા ક્રિયાપ્રતિક્રિયાઓ હોય છે, જેના કારણે સોડિયમ હાઇડ્રોક્સાઇડ દ્રાવણ સિલિકોન અણુઓનો સંપર્ક અને પ્રતિક્રિયા કરવાનું સરળ બનાવે છે.
▪ ની રચનાસિલિકોનડાયોક્સાઇડ:સિલિકોનડાયોક્સાઇડમાં સ્થિર અવકાશી નેટવર્ક માળખું છે.સિલિકોનઅણુઓ અને ઓક્સિજન પરમાણુઓ સહસંયોજક બંધનો દ્વારા ચુસ્તપણે બંધાયેલા હોય છે જેથી એક સખત અને સ્થિર સ્ફટિક માળખું બને છે. સોડિયમ હાઇડ્રોક્સાઇડ દ્રાવણ માટે તેના આંતરિક ભાગમાં પ્રવેશ કરવો અને સિલિકોન પરમાણુઓનો સંપૂર્ણ સંપર્ક કરવો મુશ્કેલ છે, જેના પરિણામે ઝડપી પ્રતિક્રિયામાં મુશ્કેલી પડે છે. સિલિકોન ડાયોક્સાઇડ કણોની સપાટી પરના સિલિકોન પરમાણુઓ જ સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા આપી શકે છે, જે પ્રતિક્રિયા દરને મર્યાદિત કરે છે.
પરિસ્થિતિઓનો પ્રભાવ
▪ સોડિયમ હાઇડ્રોક્સાઇડ સાથે સિલિકોનની પ્રતિક્રિયા: ગરમીની સ્થિતિમાં, સોડિયમ હાઇડ્રોક્સાઇડ દ્રાવણ સાથે સિલિકોનનો પ્રતિક્રિયા દર નોંધપાત્ર રીતે ઝડપી બનશે, અને પ્રતિક્રિયા સામાન્ય રીતે ઊંચા તાપમાને સરળતાથી આગળ વધી શકે છે.
▪ સિલિકોન ડાયોક્સાઇડની સોડિયમ હાઇડ્રોક્સાઇડ સાથે પ્રતિક્રિયા: સિલિકોન ડાયોક્સાઇડની સોડિયમ હાઇડ્રોક્સાઇડ દ્રાવણ સાથેની પ્રતિક્રિયા ઓરડાના તાપમાને ખૂબ જ ધીમી હોય છે. સામાન્ય રીતે, ઉચ્ચ તાપમાન અને કેન્દ્રિત સોડિયમ હાઇડ્રોક્સાઇડ દ્રાવણ જેવી કઠોર પરિસ્થિતિઓમાં પ્રતિક્રિયા દરમાં સુધારો થશે.
પોસ્ટ સમય: ડિસેમ્બર-૧૦-૨૦૨૪