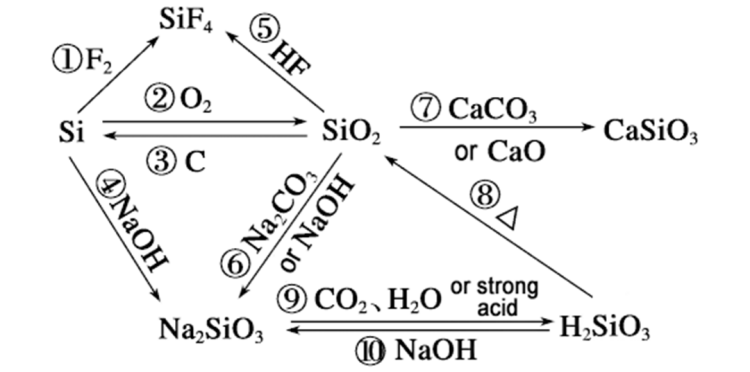
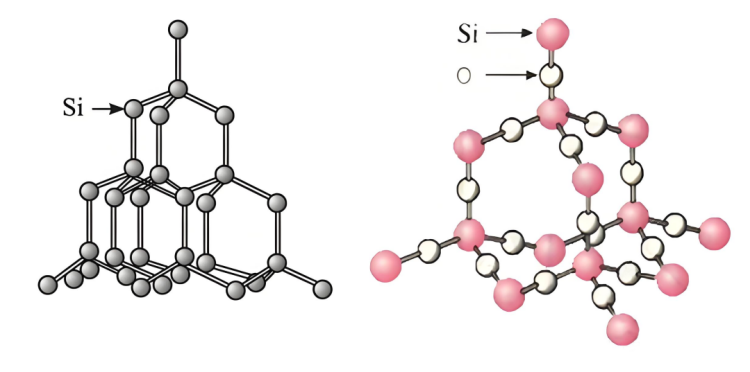
ทำไมอัตราการเกิดปฏิกิริยาของซิลิคอนและโซเดียมไฮดรอกไซด์สามารถแซงหน้าซิลิกอนไดออกไซด์ได้ โดยสามารถวิเคราะห์ได้จากประเด็นต่อไปนี้:
ความแตกต่างของพลังงานพันธะเคมี
▪ ปฏิกิริยาระหว่างซิลิกอนกับโซเดียมไฮดรอกไซด์: เมื่อซิลิกอนทำปฏิกิริยากับโซเดียมไฮดรอกไซด์ พลังงานพันธะ Si-Si ระหว่างอะตอมซิลิกอนจะอยู่ที่ 176kJ/mol เท่านั้น พันธะ Si-Si จะแตกออกระหว่างปฏิกิริยา ซึ่งแตกได้ง่ายกว่า เมื่อพิจารณาจากจลนศาสตร์ ปฏิกิริยาจะดำเนินไปได้ง่ายกว่า
▪ ปฏิกิริยาระหว่างซิลิกอนไดออกไซด์และโซเดียมไฮดรอกไซด์ พลังงานพันธะ Si-O ระหว่างอะตอมซิลิกอนและอะตอมออกซิเจนในซิลิกอนไดออกไซด์อยู่ที่ 460kJ/mol ซึ่งถือว่าค่อนข้างสูง ต้องใช้พลังงานที่สูงกว่าในการแยกพันธะ Si-O ระหว่างปฏิกิริยา ดังนั้นจึงเกิดปฏิกิริยาได้ค่อนข้างยากและอัตราการเกิดปฏิกิริยาก็ค่อนข้างช้า
กลไกการตอบสนองที่แตกต่างกัน
▪ ซิลิกอนทำปฏิกิริยากับโซเดียมไฮดรอกไซด์: ซิลิกอนทำปฏิกิริยากับโซเดียมไฮดรอกไซด์ก่อนโดยทำปฏิกิริยากับน้ำเพื่อสร้างไฮโดรเจนและกรดซิลิซิก จากนั้นกรดซิลิซิกทำปฏิกิริยากับโซเดียมไฮดรอกไซด์เพื่อสร้างโซเดียมซิลิเกตและน้ำ ระหว่างปฏิกิริยานี้ ปฏิกิริยาระหว่างซิลิกอนและน้ำจะปลดปล่อยความร้อน ซึ่งสามารถส่งเสริมการเคลื่อนที่ของโมเลกุล จึงสร้างสภาพแวดล้อมจลนศาสตร์ที่ดีกว่าสำหรับปฏิกิริยาและเร่งอัตราการเกิดปฏิกิริยา
▪ ซิลิกอนไดออกไซด์ทำปฏิกิริยากับโซเดียมไฮดรอกไซด์: ซิลิกอนไดออกไซด์ทำปฏิกิริยากับโซเดียมไฮดรอกไซด์ก่อนโดยทำปฏิกิริยากับน้ำเพื่อสร้างกรดซิลิซิก จากนั้นกรดซิลิซิกทำปฏิกิริยากับโซเดียมไฮดรอกไซด์เพื่อสร้างโซเดียมซิลิเกต ปฏิกิริยาระหว่างซิลิกอนไดออกไซด์กับน้ำนั้นช้ามาก และกระบวนการปฏิกิริยาโดยพื้นฐานแล้วจะไม่ปลดปล่อยความร้อน เมื่อมองจากมุมมองจลนศาสตร์แล้ว ซิลิกอนไดออกไซด์ไม่เอื้อต่อปฏิกิริยาที่รวดเร็ว
โครงสร้างวัสดุที่แตกต่างกัน
▪ โครงสร้างซิลิคอน :ซิลิคอนมีโครงสร้างผลึกบางชนิด และมีช่องว่างและปฏิสัมพันธ์ระหว่างอะตอมที่ค่อนข้างอ่อน ซึ่งทำให้สารละลายโซเดียมไฮดรอกไซด์สัมผัสและทำปฏิกิริยากับอะตอมซิลิกอนได้ง่ายขึ้น
▪ โครงสร้างของซิลิคอนไดออกไซด์:ซิลิคอนไดออกไซด์มีโครงสร้างเครือข่ายเชิงพื้นที่ที่มั่นคงซิลิคอนอะตอมและอะตอมออกซิเจนถูกยึดแน่นด้วยพันธะโควาเลนต์เพื่อสร้างโครงสร้างผลึกที่แข็งและเสถียร สารละลายโซเดียมไฮดรอกไซด์นั้นยากที่จะแทรกซึมเข้าไปในส่วนภายในและสัมผัสกับอะตอมซิลิกอนได้อย่างเต็มที่ ส่งผลให้ปฏิกิริยาที่เกิดขึ้นอย่างรวดเร็วทำได้ยาก มีเพียงอะตอมซิลิกอนบนพื้นผิวของอนุภาคซิลิกอนไดออกไซด์เท่านั้นที่สามารถทำปฏิกิริยากับโซเดียมไฮดรอกไซด์ได้ ทำให้อัตราการเกิดปฏิกิริยาลดลง
ผลกระทบจากเงื่อนไข
▪ ปฏิกิริยาระหว่างซิลิกอนกับโซเดียมไฮดรอกไซด์: ภายใต้สภาวะความร้อน อัตราการเกิดปฏิกิริยาระหว่างซิลิกอนกับสารละลายโซเดียมไฮดรอกไซด์จะเพิ่มขึ้นอย่างมาก และโดยทั่วไปปฏิกิริยาสามารถดำเนินไปได้อย่างราบรื่นที่อุณหภูมิสูง
▪ ปฏิกิริยาระหว่างซิลิกอนไดออกไซด์กับโซเดียมไฮดรอกไซด์: ปฏิกิริยาระหว่างซิลิกอนไดออกไซด์กับสารละลายโซเดียมไฮดรอกไซด์จะช้ามากที่อุณหภูมิห้อง โดยปกติแล้ว อัตราการเกิดปฏิกิริยาจะดีขึ้นภายใต้สภาวะที่รุนแรง เช่น อุณหภูมิสูงและสารละลายโซเดียมไฮดรอกไซด์เข้มข้น
เวลาโพสต์: 10-12-2024