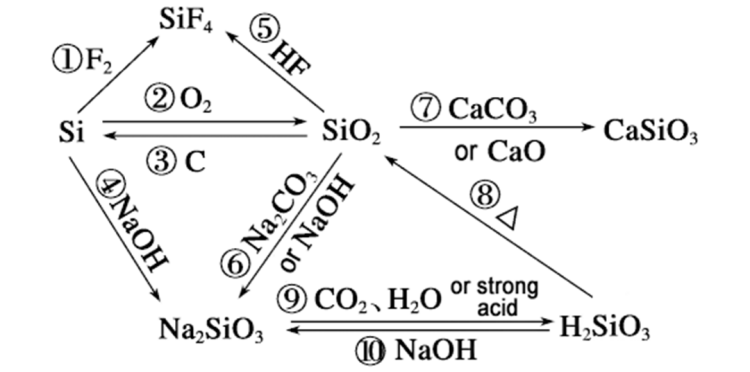
چرا سرعت واکنشسیلیکونو هیدروکسید سدیم میتواند از دی اکسید سیلیکون پیشی بگیرد، که میتوان آن را از جنبههای زیر تجزیه و تحلیل کرد:
تفاوت در انرژی پیوند شیمیایی
▪ واکنش سیلیکون و هیدروکسید سدیم: وقتی سیلیکون با هیدروکسید سدیم واکنش میدهد، انرژی پیوند Si-Si بین اتمهای سیلیکون تنها ۱۷۶ کیلوژول بر مول است. پیوند Si-Si در طول واکنش میشکند که شکستن آن نسبتاً آسانتر است. از نقطه نظر سینتیکی، ادامه واکنش آسانتر است.
▪ واکنش دی اکسید سیلیکون و هیدروکسید سدیم: انرژی پیوند Si-O بین اتمهای سیلیکون و اتمهای اکسیژن در دی اکسید سیلیکون ۴۶۰ کیلوژول بر مول است که نسبتاً زیاد است. برای شکستن پیوند Si-O در طول واکنش به انرژی بالاتری نیاز است، بنابراین وقوع واکنش نسبتاً دشوار و سرعت واکنش کند است.
مکانیسمهای واکنش مختلف
▪ واکنش سیلیکون با هیدروکسید سدیم: سیلیکون ابتدا با هیدروکسید سدیم واکنش میدهد و با آب واکنش میدهد تا هیدروژن و اسید سیلیسیک تولید کند، سپس اسید سیلیسیک با هیدروکسید سدیم واکنش میدهد تا سیلیکات سدیم و آب تولید کند. در طول این واکنش، واکنش بین سیلیکون و آب گرما آزاد میکند که میتواند حرکت مولکولی را افزایش دهد و در نتیجه محیط جنبشی بهتری برای واکنش ایجاد کند و سرعت واکنش را افزایش دهد.
▪ واکنش دیاکسید سیلیکون با هیدروکسید سدیم: دیاکسید سیلیکون ابتدا با هیدروکسید سدیم واکنش میدهد و با آب واکنش میدهد و اسید سیلیسیک تولید میکند، سپس اسید سیلیسیک با هیدروکسید سدیم واکنش میدهد و سیلیکات سدیم تولید میکند. واکنش بین دیاکسید سیلیکون و آب بسیار کند است و اساساً فرآیند واکنش گرمایی آزاد نمیکند. از نظر جنبشی، برای واکنش سریع مناسب نیست.
ساختارهای مختلف مواد
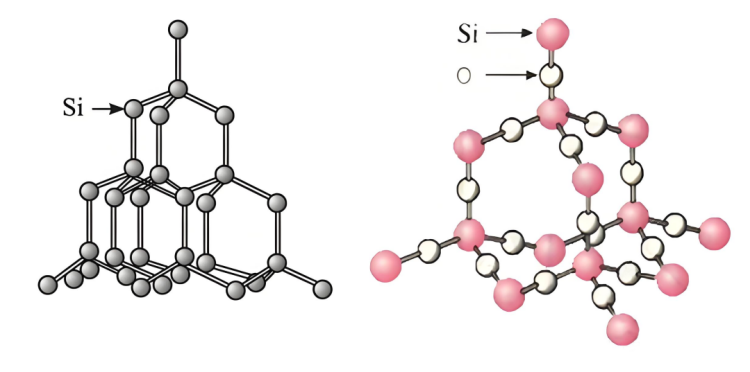
▪ ساختار سیلیکون:سیلیکونساختار بلوری خاصی دارد و شکافهای مشخص و برهمکنشهای نسبتاً ضعیفی بین اتمها وجود دارد که تماس و واکنش محلول هیدروکسید سدیم با اتمهای سیلیکون را آسانتر میکند.
▪ ساختارسیلیکوندی اکسید:سیلیکوندی اکسید کربن ساختار شبکه فضایی پایداری دارد.سیلیکوناتمها و اتمهای اکسیژن توسط پیوندهای کووالانسی محکم به هم متصل شدهاند تا یک ساختار کریستالی سخت و پایدار تشکیل دهند. نفوذ محلول هیدروکسید سدیم به داخل آن و تماس کامل با اتمهای سیلیکون دشوار است و در نتیجه واکنش سریع را با مشکل مواجه میکند. فقط اتمهای سیلیکون روی سطح ذرات دیاکسید سیلیکون میتوانند با هیدروکسید سدیم واکنش دهند و سرعت واکنش را محدود کنند.
تأثیر شرایط
▪ واکنش سیلیکون با هیدروکسید سدیم: در شرایط حرارت، سرعت واکنش سیلیکون با محلول هیدروکسید سدیم به طور قابل توجهی افزایش مییابد و واکنش عموماً میتواند در دماهای بالا به طور روان پیش برود.
▪ واکنش دی اکسید سیلیکون با هیدروکسید سدیم: واکنش دی اکسید سیلیکون با محلول هیدروکسید سدیم در دمای اتاق بسیار کند است. معمولاً سرعت واکنش در شرایط سخت مانند دمای بالا و محلول غلیظ هیدروکسید سدیم بهبود خواهد یافت.
زمان ارسال: ۱۰ دسامبر ۲۰۲۴